製品特性 | フィナステリド錠
製品特性
-
製品特性
1ジヒドロテストステロンの産生を抑制する5α-還元酵素Ⅱ型阻害薬
フィナステリドは、テストステロンをジヒドロテストステロン(DHT)に変換する5α-還元酵素Ⅱ型を阻害する作用を持ち、DHTが誘発する男性の男性型脱毛症患者において、ヘアサイクルを是正する効果を示す。
【 フィナステリド錠0.2mg・1mg「ファイザー」インタビューフォーム[2021年3月改訂(第4版)] 】
-
製品特性
2日本で最初に承認された男性型脱毛症用薬の後発医薬品
フィナステリド錠0.2mg・1mg「VTRS」は日本で最初に男性型脱毛症を適応として製造販売承認された後発医薬品である。
-
製品特性
3誤投与防止のための認識性向上の取り組み
-
包装(小函、PTPシート)にユニバーサルデザイン仕様の「つたわるフォント*」を採用することで、誤認防止と低視力状態に対応できるように可読性を高めている1 ~3)
「つたわるフォント」は一般的なフォントに比べて、低視力状態や低コントラスト状態(明るい部分と暗い部分との明暗の差があまりない状態)でも類似した文字の判別がつきやすい、ユニバーサルデザインフォント仕様になっている。
VTRS後発医薬品の新製品のパッケージやラベルは、医療用医薬品では初の試みとして、この「つたわるフォント」を採用することで、誤認防止や可読性向上に取り組んでいる。

「つたわるフォント」は慶應義塾大学、博報堂ユニバーサルデザイン、株式会社タイプバンクにより共同で開発された書体です。
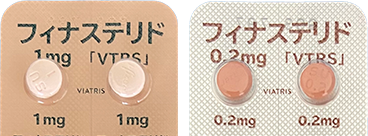
フィナステリドの小函やPTPシートには「つたわるフォント」を採用しています。


- 中野泰志ほか:「エビデンスに基づいたユニバーサルデザインフォントの開発(1)―明朝体、ゴシック体、ユニバーサルデザイン書体の可読性の比較―」:第35回感覚代行シンポジウム講演論文集:25, 2009
- 新井哲也ほか:「エビデンスに基づいたユニバーサルデザインフォントの開発(2)―低視力状態での可視性の比較―」:第35回感覚代行シンポジウム講演論文集:29, 2009
- 山本亮ほか:「エビデンスに基づいたユニバーサルデザインフォントの開発(3)―低コントラスト状態での可視性の比較―」:第35回感覚代行シンポジウム講演論文集:33, 2009
-
規格取り違えを防ぐ試みとして、複数規格の製剤は、上の規格(高用量)がある場合、記載含量の上に▲を配置し、下の規格(低用量)がある場合、記載含量の下に▼を配置している
※ 単一規格のみの場合は、記載含量を▲▼で囲んでいる


-
PTPシートのデザインを工夫することで識別性を高めている
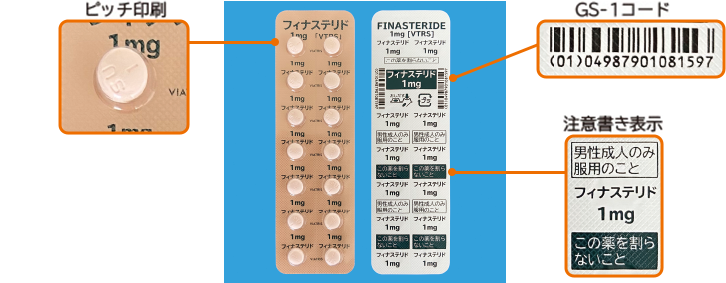
フィナステリドの錠剤には識別コードを刻印し、PTP シートには1錠単位でも成分名が分かるピッチ印刷、注意書き表示など識別性を高める工夫を行っている。また、医薬品の取り違え防止を目的として、PTP シートに1シート2バーコード(GS-1コード)を表示している。
-
改ざん防止のために小函にマイクロ文字を使用している
小函に偽薬防止策として、通常のコピーやスキャンでは再現が困難な微小な文字であるマイクロ文字を使用している。

-
-
製品特性
4安全性情報
本剤は使用成績調査等の副作用発現頻度が明確となる調査を実施していないが、フィナステリドの重大な副作用として、肝機能障害が報告されている。
主な副作用については、添付文書のその他の副作用をご参照ください。【 フィナステリド錠0.2mg・1mg「ファイザー」インタビューフォーム[2021年3月改訂(第4版)] 】
開発の経緯
フィナステリドは男性ホルモン関連疾患の治療薬として開発された4-アザステロイド化合物であり、男性型脱毛症用薬として承認を得たものである。
フィナステリド錠0.2mg・1mg「ファイザー」は、後発医薬品として開発を企画され、薬食発第0331015号(平成17年3月31日)に基づく規格及び試験方法を設定、安定性試験、生物学的同等性試験を実施し、2015年2月に承認され、同年4月に発売された製剤である(標準品名:プロペシア 製造販売元:MSD)。
【 フィナステリド錠0.2mg・1mg「ファイザー」インタビューフォーム[2021年3月改訂(第4版)] 】
「警告・禁忌を含む使用上の注意」等については DI情報をご参照ください。
DI情報をご参照ください。
