製品特性 | タダラフィル錠CI
製品特性
-
製品特性
1ホスホジエステラーゼ5(PDE5)阻害薬
タダラフィルは、ホスホジエステラーゼ5(PDE5)阻害薬である。性的興奮時に海綿体内のPDE5を抑制して陰茎の勃起と持続を助ける。
【グッドマン・ギルマン薬理書(下)薬物治療の基礎と臨床 第 12 版,廣川書店,2330,2013】
-
製品特性
2誤投与防止のための認識性向上の取り組み
-
PTPシートの工夫
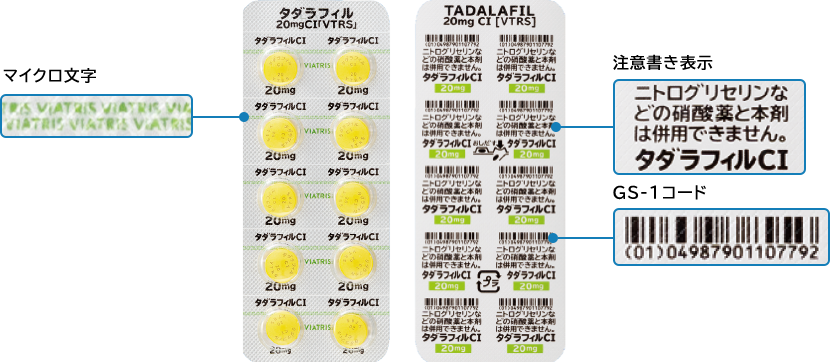
PTPシート表面には1錠単位で改ざん防止のためにマイクロ文字を使用し、不正流通を防いでいる。シート裏面には1錠単位で「ニトログリセリンなどの硝酸薬と本剤は併用できません。」の服用時の注意書き表示を記載している。また、PTPシートには分割しても「タダラフィルCI」、規格、GS-1コードが分かるピッチ印刷など識別性を高める工夫をしている。
-
包装(小函、PTPシート)にユニバーサルデザイン仕様の「つたわるフォント*」を採用することで、誤認防止と低視力状態に対応できるように可読性を高めている1 ~3)
「つたわるフォント」は一般的なフォントに比べて、低視力状態や低コントラスト状態(明るい部分と暗い部分との明暗の差があまりない状態)でも類似した文字の判別がつきやすい、ユニバーサルデザインフォント仕様になっている。
VTRS後発医薬品の新製品のパッケージやラベルは、医療用医薬品では初の試みとして、この「つたわるフォント」を採用することで、誤認防止や可読性向上に取り組んでいる。-1コードが分かるピッチ印刷など識別性を高める工夫をしている。

「つたわるフォント」は慶應義塾大学、博報堂ユニバーサルデザイン、株式会社タイプバンクにより共同で開発された書体です。
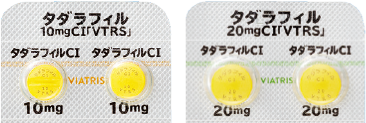
タダラフィルの小函やPTPシートには「つたわるフォント」を採用しています。


- 中野泰志ほか:「エビデンスに基づいたユニバーサルデザインフォントの開発(1)―明朝体、ゴシック体、ユニバーサルデザイン書体の可読性の比較―」:第35回感覚代行シンポジウム講演論文集:25, 2009
- 新井哲也ほか:「エビデンスに基づいたユニバーサルデザインフォントの開発(2)―低視力状態での可視性の比較―」:第35回感覚代行シンポジウム講演論文集:29, 2009
- 山本亮ほか:「エビデンスに基づいたユニバーサルデザインフォントの開発(3)―低コントラスト状態での可視性の比較―」:第35回感覚代行シンポジウム講演論文集:33, 2009
-
PTP包装の小函の開封口に、「開封済」表示を採用している
小函のGS-小函の開封口を開けると、「開封済」の文字が表示されるパッケージデザインを採用し、開封済みか一目で確認できる。

-
-
製品特性
3安全性情報
本剤は使用成績調査等の副作用発現頻度が明確となる調査を実施していないが、タダラフィル錠の重大な副作用として
過敏症(発疹、蕁麻疹、顔面浮腫、剥脱性皮膚炎、Stevens-Johnson症候群)が、ごくまれに報告されている。
主な副作用については、添付文書のその他の副作用をご参照ください。【タダラフィル錠10mgCI・20mgCI「VTRS」インタビューフォーム[2023年2月作成(第7版)]】
「警告・禁忌を含む使用上の注意」等については DI情報をご参照ください。
DI情報をご参照ください。
