点眼指導の要点
処方された点眼薬を患者さんに適正にご使用いただくための、点眼指導の要点についてご紹介します。以下は「緑内障診療ガイドライン(第5版)」に記載されている点眼指導の要点です。
点眼指導の要点
- 点眼前に手を洗う点眼瓶の先が睫毛に触れないように注意する
- 点眼は1回1滴とする
- 点眼後は静かに閉瞼し、涙嚢部を圧迫する
- 目の周りにあふれた薬液は拭き取り、手に付いた薬液は洗い流す
- 複数の点眼薬を併用するときは、5分以上の間隔を空けて点眼する

「警告・禁忌を含む注意事項等情報」等は最新の電子添文をご参照ください。
処方された点眼薬を患者さんに適正にご使用いただくための、点眼指導の要点についてご紹介します。以下は「緑内障診療ガイドライン(第5版)」に記載されている点眼指導の要点です。
点眼指導の要点
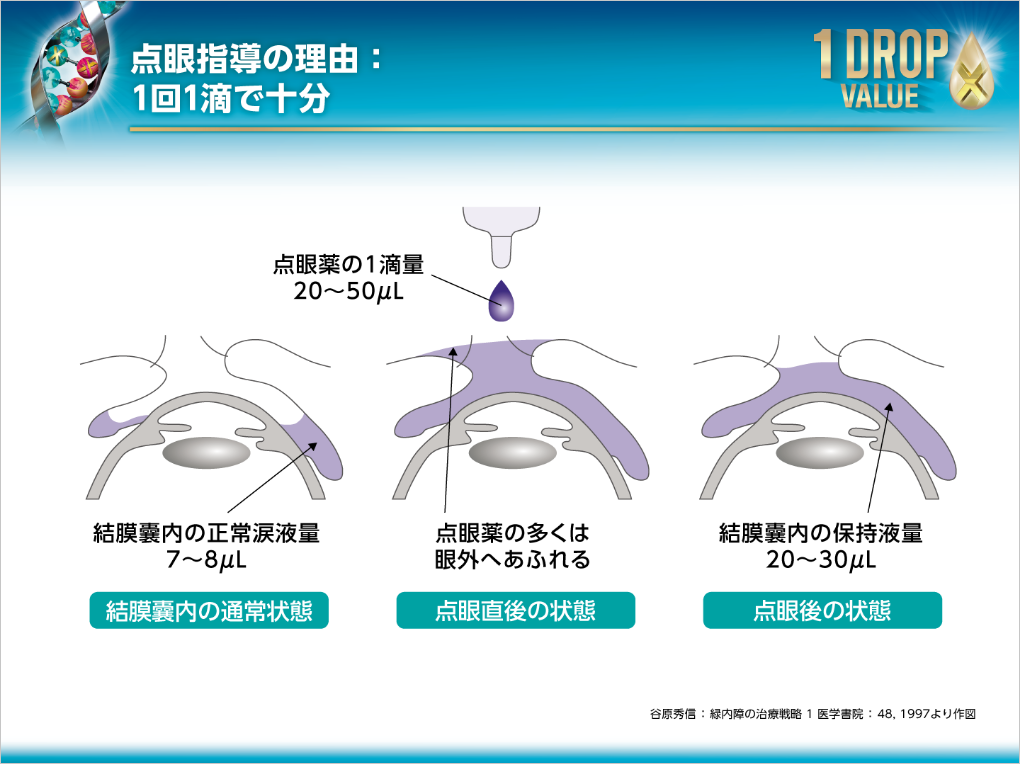
結膜嚢内の正常涙液量は7~8μLとされています。また点眼後の結膜嚢内の保持液量は20~30μLとされています。点眼薬の1滴量は20~50μLですので、点眼直後は1滴でも多くは眼外へあふれます。したがって通常は、1回に2滴以上点眼する必要はないということになります。
点眼後はまばたきをせずに約1~5分間、目を閉じておきます。さらに目頭の部分を1分以上軽く押さえておくと、薬の効きが良くなり、副作用の軽減にもつながる可能性が高まります。ただし、目頭の付近に傷や腫れのある時は、やめていただくようご指導ください。

プロスタグランジン関連薬の副作用として、眼瞼の色素沈着や発毛、睫毛が太くなったり長くなったりするというものがあります。この副作用は、あふれた薬液が付着することにより発症するので、点眼後の拭き取りをしっかりすることで防ぐことができるとされていますので、ご指導をよろしくお願いします。

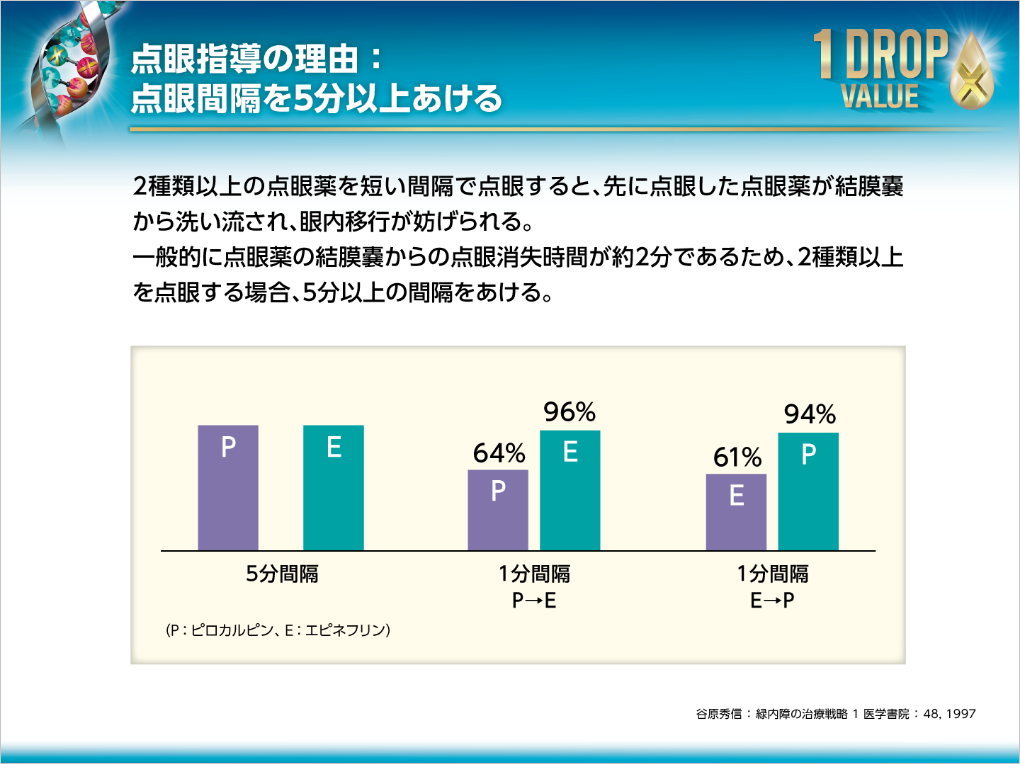
2種類以上の点眼薬を短い間隔で点眼すると、先に点眼した点眼薬が結膜嚢から洗い流され、眼内移行が妨げられると報告されています。一般的に、点眼薬の結膜嚢からの点眼消失時間が約2分であるため、2種類以上を点眼する場合、5分以上の間隔をあけるようにご指導ください。
「警告・禁忌を含む注意事項等情報」等は最新の電子添文をご参照ください。
ご利用にあたっては以下の利用条件をご覧ください。
弊社は、厚生労働省「医療用医薬品の販売情報提供活動に関するガイドライン」に則り、提供相手方のお名前・ご施設名を記録させていただいております。閲覧をご希望される際には、お名前・ご施設名を入力いただきますのでご了承ください。なお、入力いただいた情報、および閲覧された資料は、以下の利用目的の範囲で利用記録として収集、記録、保存させていただきます。収集した個人情報は以下の目的のみに利用いたします。
利用目的:情報の提供先の把握、記録、保存。
取得した個人情報の取り扱いに関しては、弊社のプライバシーポリシーをご参照ください。
一部製品において、ご提供いただいたお名前、ご施設名をヴィアトリスグループ会社間に共有させて頂くことがあります。
「Q&A*」ページには以下の情報が含まれております。ご利用に際しては、ご利用者において十分ご留意ください。
なお掲載されている全ての情報は、無断で複製すること、第三者に頒布することを禁止いたします。
*:Q&Aの一部のコンテンツは、海外で作成した資料のため日本の文献情報等が一部含まれていない場合もございます。また、最新の情報をお届けするために、要旨、電子添文情報、免責条項以外は海外で作成した英語原文での回答とさせていただいてるコンテンツもございます。
以上の事項に同意のうえ、ページを移動しますか?